本期视点
一例22岁男性患者,因肾病综合征入我院肾内科诊治,临床诊断为系统性红斑狼疮(SLE)。住院后超声心动图检查发现二尖瓣前后叶类圆形赘生物,其超声特点提示与SLE和抗磷脂抗体综合征相关的Libman-Sacks心内膜炎可能,最终经肾穿刺病理及多次抗β2糖蛋白Ⅰ抗体升高而确诊。利布曼-萨克斯(Libman-Sacks)心内膜炎须与乳头状弹性纤维瘤、感染性心内膜炎赘生物、Lambl氏赘生物、赘疣性血栓性心内膜炎和瓣膜黏液样变性等鉴别。本例提示,当年轻肾病综合征患者存在瓣膜赘生物时,应进一步寻找SLE或抗心磷脂抗体综合征的证据。
病历摘要
现病史 患者男性,22岁。因“下肢、眼睑水肿3个月,泡沫尿2个月”入院。3个月前出现双侧眼睑及双下肢可凹性水肿,晨重暮轻。2个月前开始出现尿中泡沫增多。无皮疹、光过敏、关节肿痛和口腔溃疡等。外院测血压为160/100 mmHg。血常规:白细胞 4.62×109/L,血红蛋白124 g/L,血小板114×109/L 。尿常规提示蛋白(3+)、红细胞(+)。血生化:丙氨酸氨基转移酶(ALT)18 U/L,白蛋白30 g/L,肌酐50.6 μmol/L,总胆固醇9.39 mmol/L,低密度脂蛋白胆固醇6.64 mmol/L。腹部B超:双肾弥漫性改变,右肾10.8×6.8 cm、左肾11.3×5.9 cm,皮质回声高,脾大,余(-)。我院门诊诊断为“肾病综合征”,予泼尼松60 mg/d治疗。 既往史及其他 患者发现高血压2年,未随诊血压及进行治疗,但无任何不适。个人史、婚育史、家族史无特殊。
体格、实验室与辅助检查
体格检查 血压159/103 mmHg,颈静脉无怒张,双肺呼吸音清,心界左下扩大,心率73次/分,心尖部可闻及Ⅱ~Ⅲ/6级收缩期吹风样杂音,肝脾未触及,双下肢膝以下轻度可凹性水肿。
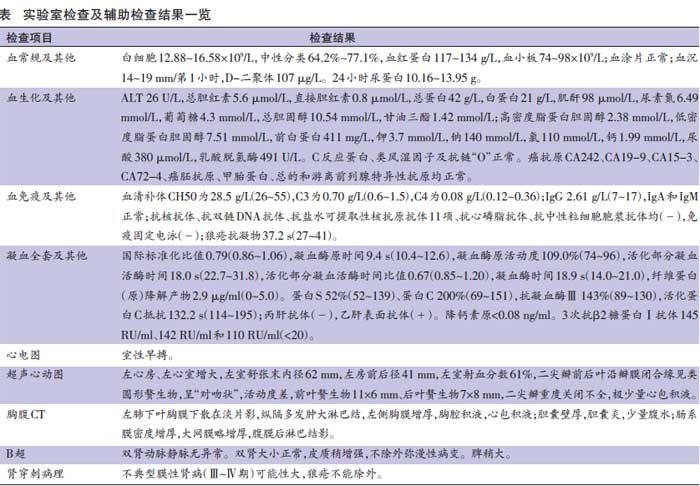
实验室检查和辅助检查 具体结果见表。
表 实验室检查及辅助检查结果一览
诊断与鉴别诊断
本例患者有以下特点:肾病综合征,二尖瓣赘生物,抗β2糖蛋白I抗体3次升高,以及肾穿刺病理提示SLE。患者存在二尖瓣赘生物,应与以下疾病鉴别。
乳头状弹性纤维瘤
乳头状弹性纤维瘤是一种心脏瓣膜最常见的原发性良性肿瘤(占10%以下),通常见于老年患者,平均发病年龄为60岁。肿瘤可发生于二尖瓣前后叶、腱索和乳头肌、主动脉瓣,但主动脉瓣较二尖瓣常见,少见部位包括三尖瓣和肺动脉瓣,亦可见于心房、心室心内膜表面,主动脉瓣的主动脉侧,二尖瓣上的左房侧。肿瘤体积小,大多数直径小于20 mm,瘤体大小范围为2~50 mm。典型肿瘤呈圆形或卵圆形,边界清楚,均质,回声强于血栓,通常为单个,亦可为多个。肿瘤常通过短蒂与心内膜表面相连,呈活动状,瓣膜功能不全不常见。超声显示肿瘤有一亮回声中心。对于呈手指样突出的肿瘤,在其与血液的界面上会出现特征性的闪动或细颤,经食管超声心动图能识别这一特点。
本例患者瓣膜上肿物活动度小,无蒂,亦未见到乳头状弹性纤维瘤的典型超声特征,且无法用该疾病解释肾病综合征。
感染性心内膜炎赘生物
感染性心内膜炎出现瓣膜赘生物常见,严重者可伴感染瓣周扩散,引起瓣膜穿孔、瓣周脓肿、窦道、瘘或假性动脉瘤等并发症,临床表现为发热、动脉栓塞等血管现象,以及肾小球肾炎等免疫现象。二尖瓣赘生物在超声心动图上常位于左房侧,典型赘生物呈不规则分叶状,边界不清,活动无序,活动频率快于瓣膜。
本例患者虽然赘生物较大,却无发热,且类风湿因子呈阴性,尿检以大量蛋白尿为特征,无贫血,加之瓣膜赘生物呈类圆形团块状、较固定,故诊断感染性心内膜炎缺乏令人信服的依据。
Lambl氏赘生物
兰布尔(Lambl)氏赘生物的发病机制尚不明确,赘生物中心为结缔组织,是胶原和弹性纤维或无细胞的透明物质,被覆内皮细胞。该疾病可见于任何年龄,但更常见于老年人,男女无差别。发生于二尖瓣的Lambl氏赘生物多于主动脉瓣,常沿瓣膜边缘的关闭线分布,可位于二尖瓣的左房侧,也可位于肺动脉瓣和主动脉瓣的任何部位,即动脉侧。Lambl氏赘生物体积小,长度为2~12 mm,宽度约1.5 mm。Lambl氏赘生物呈纤细、活动的丝状结构,有2种类型(丝状或薄层状),可为单条状、成排或成簇,常为多个。本例患者赘生物形态不符合Lambl氏赘生物,且该疾病同样无法解释肾病综合征。
瓣膜黏液样变性
明显的瓣膜黏液样变性使瓣膜增厚折叠,尤其当二尖瓣在收缩期关闭时,脱垂的瓣体部分极似赘生物,有时很难鉴别。本例患者无瓣膜脱垂,赘生物形态与黏液样变性瓣膜有区别,故可除外瓣膜黏液样变性。
赘疣性血栓性心内膜炎
该疾病又被称为肿瘤心内膜炎、休克心内膜炎或消耗性心内膜炎,属于非细菌性血栓性心内膜炎。最常见于霍奇金病,肺、胰腺、胃和结肠腺癌,亦可见于休克、弥漫性血管内凝血(DIC)、烧伤、内毒素血症和恶病质。多数侵犯左心瓣膜,心房内膜偶被累及,在心瓣膜闭锁缘形成≥1 mm的血小板血栓,有时呈息肉状。 本例患者的赘生物形态不能除外赘疣性血栓性心内膜炎,但血液检查、肿瘤标志物及胸腹影像学检查未提示肿瘤存在证据。
Libman-Sacks心内膜炎
该疾病可见于SLE和抗心磷脂抗体综合征患者,瓣膜上可形成无菌性血小板纤维素性血栓,亦属于非细菌性血栓性心内膜炎。本例患者虽然多项自身抗体阴性,无关节痛、口腔溃疡或脱发等免疫疾病表现,但患者年龄较轻,存在肾病综合征,3次查抗β2糖蛋白Ⅰ抗体均升高,抗心磷脂抗体(-),肾穿刺病理提示狼疮不除外。 抗β2糖蛋白Ⅰ抗体阳性多见于SLE和原发性抗心磷脂抗体综合征,本例患者临床表现更符合SLE,故瓣膜赘生物为Libman-Sacks心内膜炎(LSE)赘生物。
治疗
治疗宗旨
治疗主要针对SLE给予激素治疗,同时积极控制高血压,并针对蛋白尿给予双倍剂量的替米沙坦。由于患者有重度二尖瓣关闭不全伴左心扩大,有外科手术指征,但应在原发病治疗一段时间,蛋白尿被控制、低蛋白血症获得改善及激素减至一定量后,再考虑择期行外科手术,从而减少术后并发症。
治疗具体方案
泼尼松60 mg/d和复方环磷酰胺1片/天治疗原发病,同时给予阿司匹林100 mg/d,普伐他汀20 mg/d,卡维地洛6.25 mg/次、2次/天,左旋氨氯地平2.5 mg/d,氢氯噻嗪12.5 mg/d、替米沙坦80 mg/次,2次/天。患者病情逐渐缓解。
链接——认识Libman-Sacks心内膜炎
LSE的由来
1924年,伊曼纽尔·利布曼(Emanuel Libman)和本杰明·萨克斯(Benjamin Sacks)首先报告4例患者存在二尖瓣后叶心室面疣状、桑葚样赘生物,被称为LSE。LSE又称为非典型疣状心内膜炎,常见于SLE,亦可见于抗磷脂抗体综合征。LSE发生率曾被低估,随着超声心动图对赘生物探测能力的提高,LSE诊断率不断升高,达9.5%~11%。高滴度抗磷脂抗体患者是高危患者。
LSE的组织病理学
LSE在组织学上可分为活动性和陈旧性病变,前者见于年轻和初发者,赘生物由纤维素、坏死组织和单核细胞等组成,瓣膜功能受损轻;后者见于病程长的患者,赘生物为血管化的纤维组织,可伴钙化,常引起瓣膜反流。
LSE的瓣膜损害
多数 LSE患者无临床症状。最常见的瓣膜损害为瓣膜增厚,可呈弥漫性或疵状增厚。心脏各个瓣膜均可受累,以二尖瓣受累最多见,其次为主动脉瓣,肺动脉瓣和三尖瓣受累罕见。
抗磷脂抗体阳性患者发生瓣膜损害的比例高于阴性患者,说明瓣膜病变或与抗磷脂抗体有关。
在SLE引起主动脉瓣关闭不全的患者中,瓣膜可发生瓣膜炎、纤维化、类黏蛋白退行性变和穿孔,继而引起细菌性心内膜炎和主动脉夹层。SLE引起二尖瓣关闭不全的患者可发生瓣膜增厚钙化、腱索瘢痕纤维化、乳头肌类纤维蛋白坏死及腱索断裂。文献报道SLE患者进行超声心动图检查,二尖瓣和主动脉瓣受累发生率分别为63%和34%,LSE与病程、疾病活动性、抗磷脂抗体、抗磷脂综合征、血栓、卒中和血小板减少等因素相关。
在LSE的瓣膜损害中,赘生物占13%。部分患者在随访过程中的瓣膜关闭不全可加重,少数原先无赘生物的患者可出现赘生物。
LSE的赘生物特点
LSE赘生物可见于各瓣膜,二尖瓣最常见,赘生物常位于二尖瓣后叶、心室壁移行处以及瓣膜边缘,可同时累及瓣膜两面,其他部位见于瓣环、腱索、乳头肌、心房和心室内膜等处,其次为主动脉瓣。二尖瓣和主动脉瓣赘生物多于三尖瓣和肺动脉瓣,常同时累及多个瓣膜。瓣膜弥漫增厚,尤其是瓣叶中部和瓣尖。
赘生物为颗粒状致密团块,单个或聚集呈桑葚状分布于心内膜,多数较小(通常<1 cm),形态不规则,回声不均匀,在二尖瓣前后叶对称分布,呈桑葚样外观,附着于瓣膜的基底较宽,活动度差,通常没有独立活动或抖动的征象。主动脉瓣上的Libman-Sacks赘生物通常位于主动脉侧。
糖皮质激素与赘生物发病率有关,大量使用糖皮质激素治疗前的尸检发现率为59%,治疗后降为35%。激素治疗前心内膜受累面较广泛,左右心受累几率相等, 激素治疗后则多集中于左心。
LSE的并发症
LSE可并发栓塞,但赘生物一般较小且附着较紧密,故并不常见。栓塞事件与抗磷脂抗体及瓣膜病变(赘生物、增厚和关闭不全)独立相关,主要表现为卒中或短暂性脑缺血发作,偶可引起心肌梗死。
LSE可引起瓣膜功能异常,包括狭窄或关闭不全,但后者多于前者。二尖瓣狭窄时风险升高,可继发心房颤动。多数患者瓣膜功能异常较轻,无临床症状;少数患者瓣膜病变程度较重,可出现相应的瓣膜病变症状,甚至导致心力衰竭,需外科治疗。
其他治疗措施 激素和免疫抑制剂针对原发病SLE和抗磷脂抗体综合征进行治疗,但与赘生物大小变化无明确相关性。此外,预防感染性心内膜炎也很重要,以避免严重并发症。若患者存在系统性栓塞,则应给予抗凝治疗。阿司匹林的治疗作用未被充分阐明。心力衰竭、抗凝治疗后仍反复发生血栓栓塞者须进行瓣膜置换,但机械瓣易发生血栓,且二尖瓣置换术死亡率高达25%。
LSE可继发感染性心内膜炎和腱索断裂,但较罕见。
LSE与感染性心内膜炎的鉴别
LSE并发感染性心内膜炎在尸检中可达4.9%, 临床病例为1.3%,显著高于正常人或其他胶原病患者。易感因素包括瓣膜病变、肾病、网状内皮系统补体系统缺陷和激素应用。
急性LSE的许多症状与感染性心内膜炎相似,如发热、关节炎、新的杂音或甲床下出血,少数患者亦可出现严重的瓣膜关闭不全。
LSE与感染性心内膜炎的鉴别如下。LSE 瓣膜赘生物可位于多个部位,常见于二尖瓣后叶的心室侧,赘生物活动度小,回声不均匀;LSE赘生物一般不引起心脏杂音性质的改变,通常不引起临床症状,但可以脱落导致栓塞;LSE因缺乏炎症反应,瓣周结构一般不被破坏;LSE常存在抗心磷脂抗体阳性。感染性心内膜炎的赘生物沿瓣膜关闭线分布,回声均一,活动度大,呈振动和转动样,常伴有感染延伸,引起瓣周脓肿或瓣膜穿孔等并发症;感染性心内膜炎患者更易出现持续发热、明显的心脏杂音、白细胞升高或血培养阳性等表现。
LSE与感染性心内膜炎的鉴别诊断有时较困难,尤其是与血培养阴性的感染性心内膜炎相鉴别,需要结合其他临床情况进行判断。例如,一例SLE患者无发热,而二尖瓣和左心室内膜面均存在能被超声心动图检测到的活动度差的赘生物,则应考虑诊断为LSE。
(北京协和医院心内科、肾内科供稿)